En una reciente inspección llevada a cabo por el Departamento de Control de Mercado de la Dirección de Evaluación y Gestión de Monitoreo de Productos para la Salud (DEGMPS), se detectó la existencia de un desfibrilador PRIMEDIC falsificado. El hallazgo tuvo lugar durante un procedimiento de servicio técnico realizado por la empresa DRIPLAN SOCIEDAD ANÓNIMA, quien informó sobre la anomalía al organismo de control correspondiente.
SALUD
Detectan y prohíben el uso y comercialización de un desfibrilador trucho
La medida se toma con el objetivo de advertir a pacientes y profesionales sobre el riesgo que representa el uso de un producto médico falsificado.
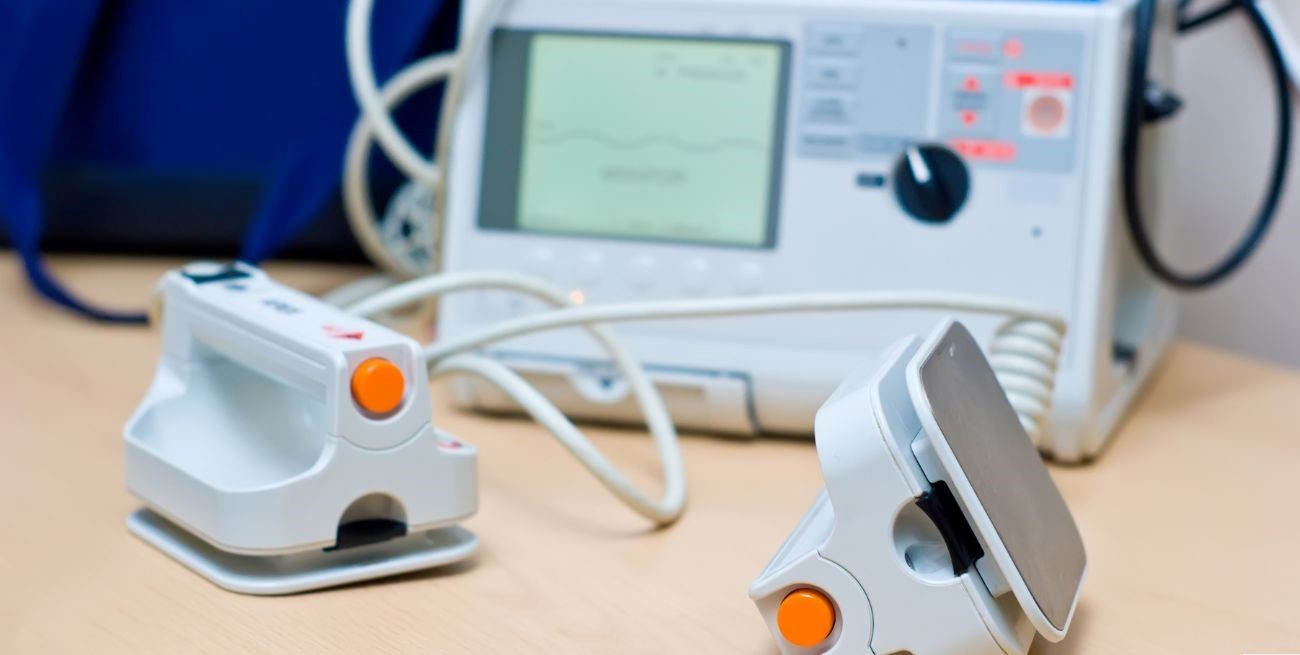
El equipo en cuestión es un desfibrilador PRIMEDIC, modelo HEART SAVE AS, registrado bajo la titularidad de DRIPLAN S.A. mediante PM N° 1608-28. Este dispositivo pertenece a la clase de riesgo III y está autorizado como desfibrilador automático externo bifásico para uso profesional o de instituciones. La DEGMPS informó que DRIPLAN S.A. es la única empresa autorizada en el país para la importación de este equipo, además de realizar el servicio técnico oficial.
La situación fue expuesta cuando, por medio del correo oficial del Departamento de Control de Mercado, se recibió la notificación de que un desfibrilador PRIMEDIC, modelo HEART SAVE AS, había sido detectado como falsificado durante un servicio técnico realizado por DRIPLAN S.A. La empresa, habilitada como importadora de productos médicos con un certificado vigente de Buenas Prácticas de Fabricación, procedió a inspeccionar el dispositivo y descubrió varias inconsistencias en los rótulos y componentes del equipo.
Durante la inspección en la sede de DRIPLAN S.A., el responsable de la firma explicó que los técnicos fueron llamados a la Cooperativa Escolar y Cultural El Palomar para realizar el mantenimiento del desfibrilador PRIMEDIC. Al examinar el equipo, modelo HEART SAVE AS, con número de serie 12357810092 y batería con número de serie 34045678003, los técnicos notaron que los rótulos adheridos al equipo y a la batería externa no coincidían con los originales de la firma. Además, los cables conectores de los parches tenían un adaptador/acople que no era propio de un equipo original.
Tras esta inspección visual, se determinó que tanto la batería externa como la pila interna estaban vencidas. Como medida inmediata, se reemplazaron la batería externa y los conectores, aunque el equipo quedó en el establecimiento bajo la condición de "No operativo". Se tomaron imágenes ilustrativas del equipo, las etiquetas/rótulos y la batería.
El 2 de mayo de 2024, personal del Departamento de Control de Mercado visitó la sede de la Cooperativa Escolar y Cultural El Palomar para verificar el estado del equipo y constató que se encontraba segregado y separado de su batería externa. Dado que se trataba de un equipo falsificado, se procedió a acondicionarlo y franjarlo para inhibir su uso, quedando bajo custodia y responsabilidad del responsable del establecimiento.
Cuando se consultó al responsable de la Cooperativa sobre la procedencia del equipo, este explicó que fue adquirido en una gestión anterior y que no contaban con documentación comercial que acreditara la adquisición. En conclusión, se determinó que la unidad detectada en el establecimiento era un equipo falsificado.
Además, el Departamento de Control de Mercado aclaró que los números de serie consignados en los rótulos del equipo y de la batería externa no existían en las unidades originales comercializadas por DRIPLAN S.A. y que las etiquetas del equipo falsificado diferían en tipografía y colores respecto a las originales.
El 10 de abril de 2024, mediante la notificación NO-2024-36350183-APN-DVPS#ANMAT, se informó al Ministerio de Salud de la provincia de Buenos Aires sobre la situación reportada por la empresa titular del registro. Se remitió el acta labrada en el establecimiento Cooperativa Escolar y Cultural El Palomar para que se tomarán las acciones correspondientes.
Mirá también
Mirá también
Se prohibió la venta de dos aceites de oliva por ser "ilegales"
Ante la gravedad del caso y con el objetivo de advertir a pacientes y profesionales sobre el riesgo que representa el uso de un producto médico falsificado, el Departamento de Control de Mercado recomendó: a) Prohibir el uso, comercialización y distribución en todo el territorio nacional del desfibrilador PRIMEDIC, modelo HEART SAVE AS, con número de serie 12357810092 y la batería PRIMEDIC con número de serie 34045678003; y b) Informar la medida a todas las autoridades sanitarias jurisdiccionales.
Finalmente, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) es competente para dictar esta disposición en virtud de las atribuciones conferidas por el Decreto No 1.490/92 y sus modificatorios. La Dirección de Evaluación y Gestión de Monitoreo de Productos para la Salud y la Coordinación de Sumarios tomaron la intervención correspondiente en el marco de sus competencias.
Disposición Oficial
ARTÍCULO 1°: Se prohíbe el uso, la comercialización y la distribución en todo el territorio nacional del producto médico falsificado: “Desfibrilador PRIMEDIC, modelo HEART SAVE AS, número de serie 12357810092, y batería PRIMEDIC con número de serie 34045678003.”




































