La Administración de Drogas y Alimentos de Estados Unidos (FDA) autorizó este lunes el tratamiento experimental con anticuerpos, llamado bamlanivimab, del laboratorio Eli Lilly & Co, para su uso en casos leves o moderados de coronavirus Covid-19.
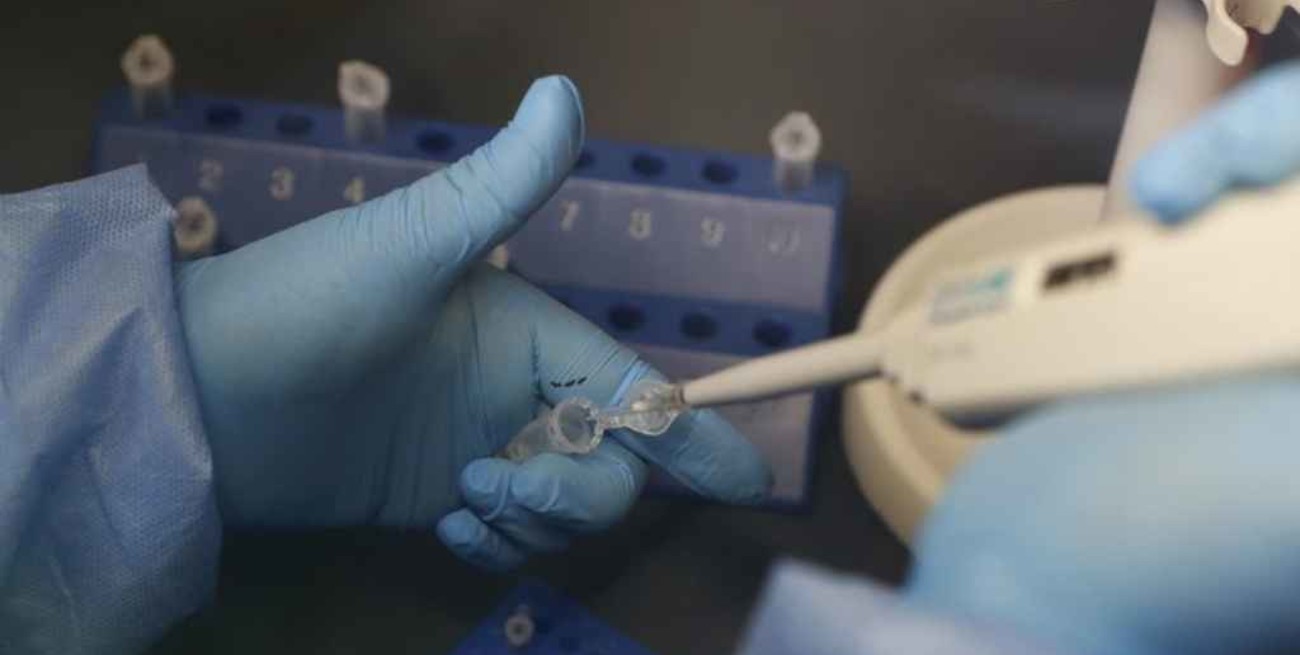
Covid-19: Estados Unidos aprueba de emergencia el tratamiento con anticuerpos monoclonales
Según anunció la agencia en su página Web, se emitió una autorización de uso de emergencia para el tratamiento, el cual es considerado útil para mantener a las personas infectadas lejos de los hospitales.
El mismo presidente Donald Trump cuando padeció la afección en octubre recibió un tratamiento basado en anticuerpos monoclonales, pero de la empresa biotecnológica Regeneron y se observó en él una rápida recuperación.
Ese tratamiento se basa en anticuerpos fabricados en laboratorios para neutralizar el coronavirus. Los resultados clínicos de los ensayos son prometedores pero su administración está restringida a esas pruebas, aunque con algunas excepciones, como la de Trump.
La autorización ofrece a los médicos una opción para combatir el virus en pacientes de alto riesgo antes de que estén lo suficientemente enfermos como para requerir hospitalización.
En tanto, otros tratamientos contra el coronavirus que recibieron el visto bueno regulatorio, como el plasma, que es un componente extraído de la sangre de pacientes con covid recuperados, y el remdesivir antiviral de Gilead Sciences, son utilizados en pacientes con covid-19 gravemente enfermos.
El presidente también fue sometido en su momento a un tratamiento con el antiviral remdesivir durante cinco días. Ese antiviral fue el primero en recibir una autorización de urgencia para su uso contra el Covid-19, el mismo que ahora se aprobó para el fármaco de Lilly.
Detalles del tratamiento

La autorización es solo para personas de 12 años o mayores con síntomas de Covid-19 pero que no requieran hospitalización. No obstante, sí debe aplicarse a aquellos cuya condición corra el riesgo de deteriorarse. Ello incluye personas mayores de 65 años y obesas, indicó la FDA. Estudios mostraron que estos demográficos son los que más pueden beneficiarse de la droga.
El tratamiento se realiza en una ocasión y se aplica por vía intravenosa. Debe realizarse lo antes posible luego de obtener un resultado positivo y dentro de los 10 días de desarrollar síntomas.
El uso de anticuerpos monoclonales es considerado uno de los tratamientos más prometedores para combatir el Covid-19. Eli Lilly y Regeneron son dos de las empresas pioneras en probarlos. Además de Lilly, laboratorios farmacéuticos en todo el mundo, como AstraZeneca, están desarrollando tratamientos similares.
La droga en cuestión, denominada LY-CoV555 o bamlanivimab, demostró éxito en personas de más de 65 años y pacientes obesos en estadios leves del Covid-19. Impidió que una infección suave a moderada del coronavirus derive en cuadros graves o complicaciones.












